Механизм гемостаза. Факторы крови участвующие в остановке кровотечения
Классический гемостатический механизм включает сосудистую реакцию, адгезию и агрегацию тромбоцитов, образование и стабилизацию сгустка, ограничение свертывания местом повреждения с помощью регуляторных антикоагулянтов и восстановление проходимости сосудов с помощью фибринолиза и заживления сосуда. В лабораторных условиях данный механизм изучается как реакция, состоящая из серии отдельных независимых событий; однако в организме эти события тесно взаимосвязаны. Например, фибриноген служит лигандом между тромбоцитами при их агрегации и является также субстратом для тромбина, образующего фибриновый сгусток. Другим примером белка, выполняющего несколько функций, является фактор Виллебранда (vWF).
Он циркулирует в комплексе с фактором VIII, где является адгезивным лигандом, склеивающим тромбоциты, а фактор VIII является одним из главных регуляторных кофакторов, контролирующих свертывание. Гемостатический механизм еще более сложен в том плане, что в организме взаимодействия могут осуществляться иными путями, чем в клинической лаборатории. Свертывание крови в условиях in vitro характеризуется такими параметрами, как АЧТВ и ПВ. ПВ отражает процесс свертывания с добавлением тканевого фактора, который вместе с фактором VII активирует фактор X. В условиях in vivo фактор VIIa активирует факторы X и IX, но в обычном клиническом лабораторном исследовании путь активации фактора IX фактором VIIa не определяется. Если бы комплекс тканевый фактор/фактор VIIa активировал бы только фактор X, было бы трудно объяснить, почему самые тяжелые нарушения кровоточивости связаны с дефицитом фактора VIII (гемофилия А) и фактора IX (гемофилия В).
Тем не менее с помощью АЧТВ и ПВ можно оценить дефицит факторов свертывания даже несмотря на то, что их физиологическая активации осуществляется отличным от лабораторного путем.
После повреждения сосуда происходит вазоконстрикция, протекающая по сосуду кровь вступает в контакт с субэндотелиальной матрицей. vWF протекающей крови входит в контакт с белками субэндотелиальной матрицы, изменяет конформацию и превращается в «клей», к которому «прилипают» рецепторы vWF на тромбоцитах. После адгезии тромбоциты активируются и выделяют накопительные гранулы, содержащие АДФ, тромбоксан А2 и другие белки, которые способствуют агрегации тромбоцитов и вовлечению других тромбоцитов в тромбоцитарную пробку. Агрегация подразумевает взаимодействие специфических рецепторов на поверхности тромбоцита с гемостатическими белками плазмы, главным образом с фибриногеном.
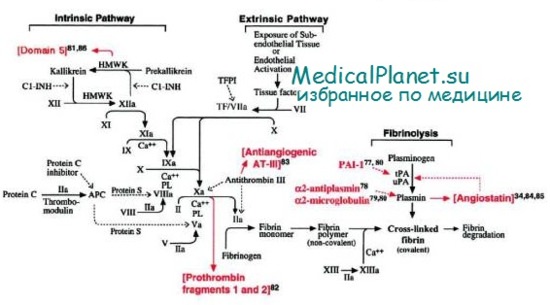
При активации тромбоцитов внутренние фосфолипиды тромбоцитов (в основном, фосфадилсерин) выходят на поверхность и взаимодействуют в двух специфических фазах процесса свертывания, включающих в себя кофакторы — фактор VIII («теназный» комплекс) и фактор V (протромбиназный комплекс). Кроме того, поврежденный сосуд выделяет тканевый фактор, происходит изменение поверхности сосуда, что инициирует каскад свертывания, который заканчивается образованием фибринового сгустка. После ретракции сгустка и формирования в нем сети поперечных фибриновых волокон с участием фактора XIII окончательно образуется стабильная фибрино-тромбоцитарная пробка.
Активированные факторы свертывания взаимодействуют друг с другом по типу так называемого каскада. Каждый активированный фактор свертывания (обозначен римскими цифрами) последовательно инициирует активацию следующего фактора свертывания. В результате процесс усиливается и происходит как бы «взрыв» свертывания крови в том месте, где это физиологически необходимо. В условиях in vivo всегда имеет место аутокатализ фактора VII с непрерывным образованием этого фактора в малых количествах, что поддерживает систему в состоянии готовности. Свертывание контролируется белками, ингибирующими коагуляцию.
Выделение тканевого фактора в месте повреждения сосуда тысячекратно усиливает генерацию фактора VIIa. На поверхности мембраны тромбоцитов, активированных в месте повреждения, очень близко друг к другу располагаются активированный фактор свертывания, его субстрат (следующий элемент каскада) и его кофактор. Такое близкое соседство максимально повышает эффективность реакций и обеспечивает взрывоподобное свертывание крови в том месте, где это нужно. Выделенный тромбин усиливает эти реакции, обеспечивая положительную обратную связь, активирующую дополнительные молекулы факторов XI, VIII и V, а также агрегируя дополнительные тромбоциты.
В клинической лаборатории фактор XII активируется с помощью поверхностного (кварц или стекло) или контактного активатора. Фактор VII активируется и взаимодействует с тканевым фактором через аналогичный каскад. Первый путь измеряется АЧТВ, второй — ПВ. Этот процесс ускоряется взаимодействием с фосфолипидом и кальцием на этапах, когда действуют факторы VIII и V. Дефицит факторов свертывания отражается в удлинении АЧТВ или ПВ по отдельности либо одновременно. Это позволяет выявить наследственный дефицит факторов свертывания; однако при приобретенных нарушениях гемостаза часто наблюдается дефицит более чем одного фактора, поэтому в этом случае оценивается относительное пролонгирование АЧТВ и ПВ.
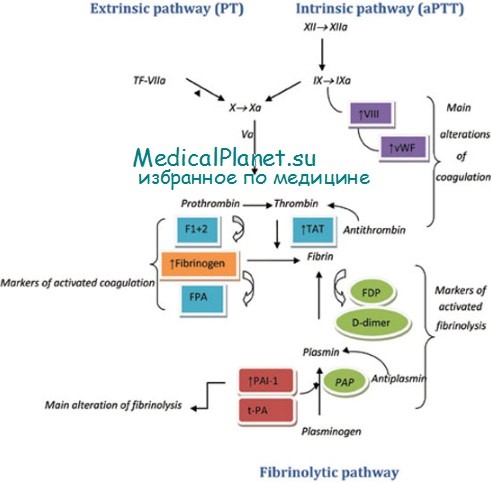
Хотя факторы свертывания названы в порядке их открытия, этот порядок не обязательно отражает последовательность их активации. Впоследствии было установлено, что факторы III, IV и VI не являются самостоятельными белками, поэтому эти термины больше не используются. Активация свертывания может осуществляться двумя путями: внутренним (активация поверхностью) и внешним (через тканевый фактор). Внутренний путь начинается с активации фактора XII, которая ускоряется двумя другими белками плазмы — прекалликреином и высокомолекулярным кининогеном. Активированный фактор XII (ХIIа), в свою очередь, активирует фактор XI, превращая его в ХIа, который катализирует превращение фактора IX в IХа. На поверхности фосфолипидной мембраны тромбоцита фактор IХа образует комплекс с фактором VIII и кальцием, который активирует фактор X («теназный» комплекс). Внешняя система (внешний путь) измеряется ПВ. Добавление тканевого фактора вызывает взрывоподобное образование фактора VIIa. Комплекс тканевый фактор/фактор VIIa активирует фактор X.
Это путь in vitro, но in vivo комплекс тканевый фактор/фактор VIIa активирует фактор IX. Независимо от способа активации фактора X (внешнего или внутреннего), результатом является образование фактора Ха, который формирует на фосфолипидной поверхности тромбоцита комплекс с фактором V и кальцием («протромбиназный» комплекс), превращающий протромбин в тромбин (называемый также фактором На). После образования тромбина фибриноген превращается в фибриновый сгусток. Этот рыхлый сгусток затем «прошивается» фактором XIII (трансглутаминазой), который образует в ней сеть поперечных волокон. На рисунке схема гемостаза показана в очень упрощенном виде, потому что Ха может активировать как фактор VIII, так и фактор V, а тромбин активирует факторы V, VIII, XI и тромбоциты. После того как тромбин активирует систему прокоагулянтов, он связывается с тромбомодулином на поверхности интактной эндотелиальной клетки, где он активирует систему антикоагулянтов. Тромбин, связанный с тромбомодулином, больше не является прокоагулянтом, но действует как антикоагулянт, активируя протеин С. Активированный протеин С инактивирует фактор V и фактор VIII, что, в свою очередь, ограничивает дальнейшее образование тромбина. Таким образом, когда тромбин встречается с интактным эпителием, он уже активирует механизм антикоагуляции и ограничивает свертывание крови.
Фактически почти все белки-прокоагулянты уравновешены белками-антикоагулянтами, и это равновесие регулирует или ингибирует функцию прокоагулянтов. Существует четыре клинически значимых естественных антикоагулянта, которые регулируют процесс свертывания. Это АТ-III, протеины С и S и ингибитор пути тканевого фактора. Основная функция АТ-III заключается в контролировании фактора Ха и тромбина. Он также может контролировать IXa, XIa и ХIIа, но это менее важная его функция. В присутствии тромбина, связанного с тромбомодулином, протеин С превращается в активированный протеин С. В присутствии кофактора протеина S активированный протеин С расщепляет и инактивирует активированный фактор V и активированный фактор VIII. Конечным ингибитором является ингибитор пути тканевого фактора, который быстро прекращает активацию фактора X фактором VII и тканевым фактором и переносит точку активации тканевого фактора и фактора VII на фактор IX.
Как только образуется стабильная фибрино-тромбоцитарная пробка, фибринолитическая система ограничивает свою деятельность этой пробкой и расщепляет ее (фибринолиз), восстанавливая целость сосуда. Плазмин, образуемый из плазминогена с участием урокиназы или тканевого активатора плазминогена (ТАП), расщепляет фибриновую пробку, в результате чего образуются продукты деградации фибрина (ПДФ). Этот путь контролируется ингибиторами активатора плазминогена типа 1 (ИАП-1) и а2-антиплазмином.
Видео схема гемостаза - механизмы внешнего и внутреннего пути
- Рекомендуем далее ознакомиться со статьей "Сбор анамнеза у детей с нарушениями гемостаза"
Оглавление темы "Нарушения в системе крови у детей":- Приобретенная панцитопения. Причины
- Лечение приобретенной панцитопении. Прогноз
- Переливание эритроцитов и эритропоэтина новорожденным, детям
- Переливание тромбоцитов новорожденным, детям
- Переливание нейтрофилов (гранулоцитов) новорожденным, детям
- Переливание свежезамороженной плазмы новорожденным, детям. Показания к переливанию СЗП
- Риски переливания крови новорожденным, детям
- Нарушения гемостаза у детей. Геморрагические заболевания
- Механизм гемостаза. Факторы крови участвующие в остановке кровотечения
- Сбор анамнеза у детей с нарушениями гемостаза

