Клиника и прогноз нейробластомы у ребенка
У детей младше 2 лет с нейробластомами обычно наблюдают выпуклый живот (из-за присутствия новообразования в брюшной полости), лихорадку и потерю массы тела. У детей старшего возраста нейробластомы могут оставаться незамеченными до тех пор, пока не возникнут гепатомегалия, асцит, дыхательные и желудочно-кишечные расстройства, боли в костях в связи с метастазированием. Нейробластомы дают распространенные метастазы лимфогенным и гематогенным путями, как правило в печень, легкие и кости, а также в костный мозг.
Могут также присутствовать проптоз и экхимоз, т.к. метастазы часто поражают периорбитальную область. Дисфункция мочевого пузыря и кишечника может быть вызвана параспинальными нейробластомами, которые поражают нервные сплетения. У новорожденных диссеминированные нейробластомы могут проявляться в виде множественных метастазов в кожу с изменением ее цвета (появлением синего оттенка, вследствие чего родилось неудачное название «ребенок, похожий на черничный пирог»).
Около 90% нейробластом независимо от их локализации продуцируют катехоламины (как и феохромацитома), в результате в крови повышаются уровни катехоламинов и их метаболитов, таких как ванилилминдальная и гомованилиновая кислоты, что является важным диагностическим критерием. Несмотря на выработку катехоламинов, гипертензия при этих опухолях развивается гораздо реже, чем при феохромацитомах. Ганглионевромы, в отличие от злокачественных нейробластом, имеют тенденцию к формированию больших бессимптомных масс и возникновению симптомов сдавления.
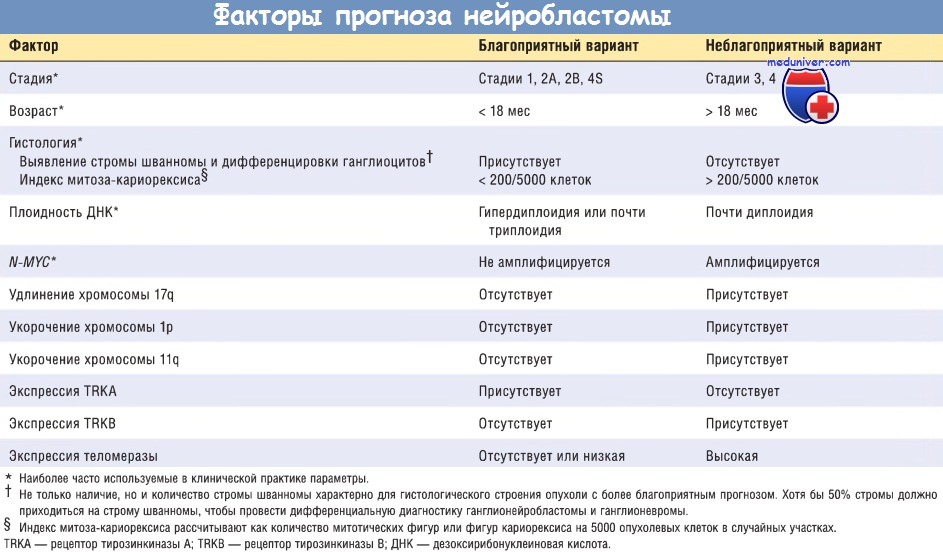
Прогноз нейробластом чрезвычайно вариабелен. Некоторые клинические, гистопатологические, молекулярные и биохимические факторы были рассмотрены в качестве проностических, на основании их пациенты были классифицированы на имеющих низкий, средний и высокий риск. При успешной терапии у первых двух категорий долгосрочный прогноз выживаемости составляет 80-90%, в то время как в группе высокого риска — менее чем 40%. Наиболее прогностически значимые факторы нейробластом:
- возраст пациента и стадия опухолевого процесса. Нейробластомы на стадиях 1, 2А или 2В имеют хороший прогноз независимо от возраста (низкий или средний риск); единственное исключение из этого правила касается опухолей с амплификацией онкогена N-MYC. Дети до 1 года с локализованной первичной опухолью и распространенными метастазами в печень, костный мозг, кожу (стадия 4S) представляют собой особую группу, у которой заболевание способно к спонтанному регрессу. Биологические основы такого поведения опухоли пока неизвестны.
Возраст 18 мес является критической точкой для прогноза. Дети моложе 18 мес имеют превосходный прогноз выживания независимо от стадии опухоли. Дети старше 18 мес попадают в группу среднего риска, в то время как высокая стадия опухоли или прогностические неблагоприятные факторы, например амплификация N-MYC в опухолевых клетках, свидетельствуют о высоком риске и плохом прогнозе;
- морфология. Это независимый прогностический фактор для нейробластических опухолей. Недавно была предложена классификация опухолей по морфологическому «возрасту», которая предусматривает разделение опухолей на благоприятные и неблагоприятные гистологические варианты;
- амплификация онкогена N-MYC. Молекулярное событие, оказывающее, возможно, самое большое влияние на прогноз, особенно для опухолей, которые изначально имели благоприятный прогноз. Появление амплификации N-MYC сразу переводит пациента в группу высокого риска независимо от его возраста, стадии и гистологии опухоли. N-MYC располагается дистально на коротком плече 2-й хромосомы (2р23-р24). Амплификация N-MYC кариотипически выявляется не в области хромосомы 2р23-р24, а, скорее, как экстрахромосомные двойные маленькие тела хроматина или гомогенно окрашиваемые области на других хромосомах. Амплификация N-MYC присутствует в 20-30% первичных опухолей, в основном на поздней стадии, при этом амплификация коррелирует с худшим прогнозом.
Амплификация N-MYC в настоящее время является наиболее частой генетической патологией, которую используют в стратификации риска нейробластических опухолей;
- плоидностъ опухолевых клеток. Коррелирует с прогнозом у детей до 2 лет, но в более старшем возрасте теряет свою независимую прогностическую ценность.
В широком смысле нейробластомы могут быть разделены на две категории: близкие к диплоидным и близкие к триплоидным (гипердиплоидные), при этом последние ассоциируются с лучшим прогнозом.
Установлено, что гипердиплоидные нейробластомы имеют нарушения механизма митоза, ведущий к нерасхождению хромосом, но при этом выявляется стабильный кариотип. Напротив, более агрессивная, близкая к диплоидной, опухоль имеет генерализованную геномную нестабильность с множественными несбалансированными транслокациями и хромосомными перестройками, которые сохраняют почти полную плоид-ность, но в результате формируется сложный кариотип с неблагоприятными прогностическими последствиями.
Итак, возраст, стадия, статус N-MYC, гистология и плоидность опухолевых клеток в настоящее время — основные критерии для стратификации риска и определения методов лечения нейробластом. Известны также некоторые молекулярные особенности, влияющие на прогноз.
Наиболее важные из них:
- гемизиготная делеция дистального отдела короткого плеча 1-й хромосомы в области р36. Обнаруживается в 25-35% первичных опухолей. Утрата 1р36 в нейробластомах имеет устойчивую корреляцию с амплификацией N-MYC, а также стадией заболевания и увеличением риска рецидива болезни в локализованных опухолях. Гемизиготная делеция генетического материала в хромосоме 11q — другой неблагоприятный прогностический фактор. Ряд микроскопических исследований позволил предположить, что эта делеция является наиболее часто встречающейся аномалией в нейробластомах;
- частичное увеличение дистального участка длинного плеча 17-й хромосомы. Выявляется в 50% опухолей и ассоциируется с неблагоприятным прогнозом, особенно с риском рецидивов в локализованных опухолях без амплификации N-MYC;
- экспрессия специфических нейротрофиновых рецепторов. Нейротрофиновые рецепторы — это семейство тирозинкиназных рецепторов, в частности TRKA, TRKB и TRKC (также известный как NTRK3), регулирующих рост, развитие и дифференцировку нервных клеток. Высокая экспрессия TRKA в нейробластомах — благоприятный прогностический маркер, ассоциированный с ранней стадией опухоли и отсутствием амплификации N-MYC. В противоположность этому повышение экспрессии TRKB в опухолях коррелирует с неблагоприятными биологическими характеристиками, включая амплификацию N-MYC, и свидетельствует о более тяжелой стадии болезни.
Хотя обсуждение методов лечения нейробластом находится за рамками этой книги, упомянем два многообещающих подхода, которые на данный момент оценивают экспериментально. Первый подход заключается в применении ретиноидов в качестве дополнительной терапии, приводящей к дифференцировке нейробластомы. Напомним, что сигнальный путь ретиноевой кислоты играет исключительную роль для клеточной дифференцировки в процессе эмбриогенеза. Другой подход — таргетная терапия, направленная на разрушение в нейробластомах онкогенных TRKB путем использования молекул-ингибиторов их тиро-зинкиназной активности. Наконец, необходимо упомянуть о скрининговых программах для нейробластом.
Поскольку огромное количество нейробластом вырабатывают катехоламины, попадающие в кровь, обнаружение метаболитов катехоламинов в моче (ванилилминдальной и гомованилиновой кислот) помогло бы выявлять детей, у которых опухоли, если они есть, имеют бессимптомное течение. Однако в двух больших исследованиях в Европе и Северной Америке не было показано улучшения показателей летальности при проведении такого скрининга, т.к. обнаруженные опухоли имели благоприятные биологические характеристики, и затраты на скрининг не оправдали его результаты. Таким образом, скрининговые программы для нейробластом в настоящее время не пропагандируют.
- Рекомендуем ознакомиться со следующей статьей "Морфология и механизмы развития опухоли Вильмса"
Оглавление темы "Патогенез детских болезней":- Причины и факторы риска синдрома внезапной детской смерти (СВДС)
- Морфология и механизмы развития синдрома внезапной детской смерти (СВДС)
- Виды доброкачественных опухолей у детей
- Виды злокачественных опухолей у детей
- Причины, морфология и стадии нейробластомы
- Клиника и прогноз нейробластомы у ребенка
- Морфология и механизмы развития опухоли Вильмса
- Клиника и прогноз опухоли Вильмса у ребенка

