Клетки иммунной системы
Прежде чем описывать нормальный и патологический иммунные ответы, необходимо обобщить важнейшие характеристики основных компонентов, участвующих в иммунном ответе.
Хотя морфологически лимфоциты ничем не примечательны и похожи один на другой, в действительности они весьма гетерогенны и их молекулярные свойства и функции специализированны. Основные классы лимфоцитов и их функции в приобретенном иммунитете показаны на рисунке ниже.
Лимфоциты и другие клетки, участвующие в иммунном ответе, не фиксированы в тканях (в отличие от клеток большинства органов), а способны мигрировать из одного лимфоидного органа в другой, а также в другие органы по кровеносным и лимфатическим путям. Это дает лимфоцитам возможность находиться в любом месте инфекции.
В лимфоидных органах лимфоциты различных классов анатомически разделены и могут взаимодействовать друг с другом лишь после активации антигенами или под влиянием других стимулов. Зрелые лимфоциты, которые не встречались со специфическим антигеном, называют наивными (т.е. иммунологически «не обученными»).
После активации в результате процесса распознавания антигена и под влиянием других сигналов лимфоциты дифференцируются в эффекторные клетки, выполняющие функцию элиминации микробов, и клетки памяти, которые существуют в состоянии готовности и лучше, чем наивные лимфоциты, приспособлены к борьбе с микробами в случае повторной инфекции. Процесс дифференцировки лимфоцитов в эффекторные клетки и клетки памяти описан далее.
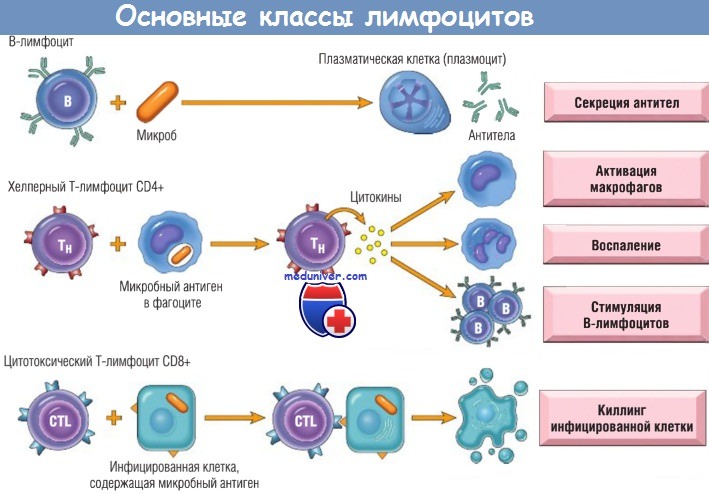
а) Т-лимфоциты. Т-лимфоциты (называемые также Т-клетками) образуются из клеток-предшественников в тимусе (Т — от thymus — тимус). Зрелые Т-клетки обнаруживаются в крови, где они составляют от 60 до 70% лимфоцитов, а также в Т-клеточных зонах периферических лимфоидных органов. Каждая Т-клетка распознает специфический, связанный с клеткой антиген с помощью антиген-специфического Т-клеточного рецептора (TCR). У = 95% Т-клеток TCR представляет собой гетеродимер, полипептидные а- и b-цепи которого соединены дисульфидной связью.
Каждая цепь состоит из вариабельной (антигенсвязывающей) и константной областей. a-TCR и b-TCR распознают пептидные антигены, представленные молекулами главного комплекса гистосовместимости (МНС) на поверхности антигенпрезентирующих клеток (АПК). Из-за того что специфичность Т-клеток ограничена пептидами, презентированными молекулами МНС на клеточной поверхности (феномен МНС-рестрикции), Т-клетки иммунной системы распознают только ассоциированные с клетками антигены (т.е. микробные антигены, присутствующие в клетках).
Разнообразие TCR возникает вследствие соматической перестройки генов, кодирующих а- и b-цепи TCR. Все клетки организма, включая клетки-предшественники лимфоцитов, содержат TCR-гены в зародышевой (гаметной) конфигурации, которые не могут быть экспрессированы в виде TCR-белков. В течение развития Т-клеток в тимусе TCR-гены перестраиваются, образуя множество различных комбинаций, которые транскрибируются и транслируются в функциональные антигенные рецепторы.
Фермент, присутствующий в созревающих лимфоцитах и опосредующий перестройку генов антигенного рецептора, представляет собой продукт RAG-1 и RAG-2 (генов, активирующих рекомбинацию); наследуемый дефект белков RAG дает в результате недостаточную генерацию зрелых лимфоцитов. Хотя каждая Т-клетка экспрессирует молекулы TCR одной специфичности, полный набор Т-клеток индивида способен распознавать чрезвычайно большое число антигенов.
Важно отметить, что зародышевые TCR-гены присутствуют во всех клетках организма, но лишь Т-клетки содержат перестроенные TCR-гены. В связи с этим наличие перестроенных TCR-генов, которые можно определить с помощью молекулярного анализа, служит маркером линии Т-клеток. Поскольку каждая Т-клетка и ее потомки, образующие клон, обладают уникальной перестроенной ДНК (а соответственно, и уникальными TCR), можно отличить поликлональную (неопухолевую) пролиферацию Т-клеток от моноклональной (опухолевой) пролиферации этих клеток. Таким образом, анализ перестроек генов антигенного рецептора служит важным методом определения опухолей лимфоидной ткани.
Каждый TCR нековалентно связан с 5 полипептидными цепями, образующими CD3-комплекс, и димером ζ-цепей. Белки CD3 и ζ являются инвариантными (т.е. идентичными) во всех Т-клетках. Эти белки участвуют в передаче сигнала в Т-клетки после связывания TCR с антигеном. Вместе с TCR они образуют TCR-комплекс.
Небольшая субпопуляция зрелых Т-клеток экспрессирует TCR другого типа, построенный из поли-пептидных у- и 8-цепей. y-TCR и δ-TCR распознают пептиды, липиды и небольшие молекулы, не нуждаясь в их презентации МНС-белками. у-Т-клетки и δ-Т-клетки обладают тенденцией скапливаться на поверхности эпителия, в частности кожи и слизистой оболочки ЖКТ и мочеполовых путей, что указывает на возможную роль этих клеток в защите от проникновения микробов через эпителий.
Однако функции у-Т-клеток и δ-Т-клеток неизвестны. Другая небольшая субпопуляция Т-клеток экспрессирует маркеры, обнаруженные на NK-клетках. Такие клетки получили название NK-T-клеток. TCR NK-T-клеток распознают гликолипиды, которые презентируют молекулы CD1, подобные молекулам МНС. Функции NK-T-клеток недостаточно хорошо выяснены.
Помимо белков CD3 и ζ Т-клетки экспрессируют некоторые другие белки, способствующие функциональному ответу TCR-комплекса. К ним относятся молекулы CD4, CD8, CD2, интегрины и CD28. CD4 и CD8 экспрессированы двумя взаимоисключающими субпопуляциями а-Т-клеток и b-Т-клеток. Молекулу CD4 экспрессируют 60% Т-клеток CD3+, которые функционируют в качестве секретирующих цитокины хелперных клеток, помогающих макрофагам и В-лимфоцитам в борьбе с инфекциями, тогда как молекулу CD8 экспрессируют 30% Т-клеток, функционирующих как цитотоксические Т-лимфоциты и разрушающих инфицированные клетки организма-хозяина.
Молекулы CD4 и CD8 служат корецепторами при активации Т-клеток и названы так потому, что участвуют в ответе на антиген вместе с антигенным рецептором. Во время презентации антигена молекулы CD4 связываются с молекулами МНС класса II, презентирующими антиген, a CD8 — с молекулами МНС класса I. При распознавании антигена антигенным рецептором Т-клеток корецепторы CD4 или CD8 инициируют сигналы, необходимые для активации Т-клеток. В результате потребности в корецепторах хелперные Т-клетки CD4+ могут распознавать и отвечать на антиген, презентированный только молекулами МНС класса II, тогда как цитотоксические Т-лимфоциты CD8+ распознают связанные с клетками антигены только в ассоциации с молекулами МНС класса I.
Для иммунного ответа необходимо, чтобы Т-клетки не только распознали комплекс антиген-МНС, но также получили сигналы от АПК. Эти процессы будут рассмотрены позже, при описании этапов клеточноопосредованного иммунного ответа.
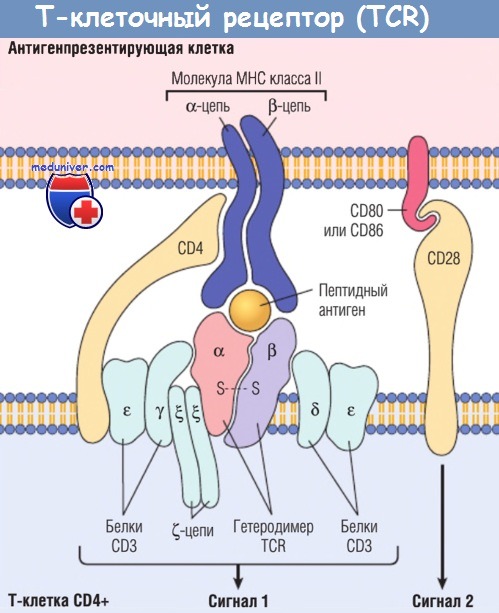
Гетеродимер TCR, состоящий из а- и P-цепей, распознает антиген (в форме комплекса пептид-МНС, экспрессированного антигенпрезентирующими клетками).
Связанный с ним CD3-комплекс и ζ-цепи инициируют активирующие сигналы.
Молекулы CD4 и CD28 также участвуют в активации Т-клеток (некоторые Т-клетки экспрессируют не CD4, a CD8; эти молекулы выполняют аналогичные функции). Величина молекул дана в произвольном масштабе. МНС — главный комплекс гистосовместимости.
б) В-лимфоциты. В-лимфоциты развиваются из костномозговых клеток-предшественников (В — от англ. bone marrow — костный мозг). Зрелые В-клетки составляют от 10 до 20% циркулирующих периферических лимфоцитов и присутствуют также в периферических лимфоидных органах — лимфатических узлах, селезенке и лимфоидной ткани слизистых оболочек.
В-клетки распознают антигены с помощью В-клеточного антигенного рецепторного комплекса. Мембраносвязанные антитела классов IgM и IgD, присутствующие на поверхности всех наивных В-клеток, представляют собой антигенсвязывающий компонент В-клеточного рецепторного комплекса. Как и в случае Т-клеток, каждый В-клеточный рецептор имеет уникальную антигенную специфичность, приобретенную в результате опосредованной RAG перестройки генов Ig.
Аналогично ситуации с Т-клетками анализ перестройки генов Ig имеет значение для идентификации моноклональных В-клеточных опухолей. После стимуляции антигеном и другими сигналами В-клетки дифференцируются в плазматические клетки, секретирующие антитела, медиаторы гуморального иммунитета. В дополнение к мембранным Ig В-клеточный антигенный рецепторный комплекс содержит гетеродимер двух инвариантных белков — Iga и Igb. Подобно белкам CD3 и ζ TCR-комплекса, Iga и Igb участвуют в передаче сигнала через антигенный рецептор. В-клетки экспрессируют также различные другие молекулы, существенные для иммунного ответа, — рецепторы системы комплемента, Fc-рецепторы и молекулы CD40.
Рецепторы системы комплемента типа 2 (CR2, или CD21) служат также рецепторами вируса Эпштейна-Барр (EBV), поэтому он легко инфицирует В-клетки.
в) Дендритные клетки. Существует два морфологических типа дендритных клеток, которые отличаются функционально. И те и другие имеют многочисленные тонкие цитоплазматические отростки, напоминающие дендриты, за что клетки и получили свое название. Клетки одного морфологического типа называют интердигитирующими дендритными клетками или просто дендритными клетками. Эти клетки представляют собой наиболее важные АПК, инициирующие первичный ответ Т-клеток на белковые антигены. Ключевая роль дендритных клеток в презентации антигена обусловлена несколькими их свойствами.
Во-первых, они расположены в стратегически важном месте, где происходит захват антигенов, — под эпителием, куда обычно попадают микробы и чужеродные антигены, и в интерстиции всех тканей, где могут продуцироваться антигены. Незрелые дендритные клетки в эпидермисе называют клетками Лангерганса. Во-вторых, дендритные клетки экспрессируют ряд рецепторов для взаимодействия с микробами (и другими антигенами) и ответа на них, включая TLR и маннозные рецепторы. В-третьих, в ответ на микробы дендритные клетки мобилизуются в Т-клеточные зоны лимфоидных органов, т.е. в идеальное место для презентации антигенов Т-клеткам. В-четвертых, дендритные клетки экспрессируют на высоком уровне молекулы, необходимые для презентации антигенов и активации Т-клеток CD4+.
Клетки другого морфологического типа присутствуют в зародышевых центрах лимфоидных фолликулов селезенки и лимфоузлов, поэтому эти клетки называют фолликулярными дендритными клетками. Они несут Fc-рецепторы для IgG и рецепторы для С3b и могут захватывать антигены, связанные с антителами или белками системы комплемента. Такие клетки участвуют в гуморальном иммунном ответе, презентируя антигены В-клеткам и осуществляя отбор В-клеток, обладающих наивысшей аффинностью к антигену, что приводит к образованию высококачественных антител.
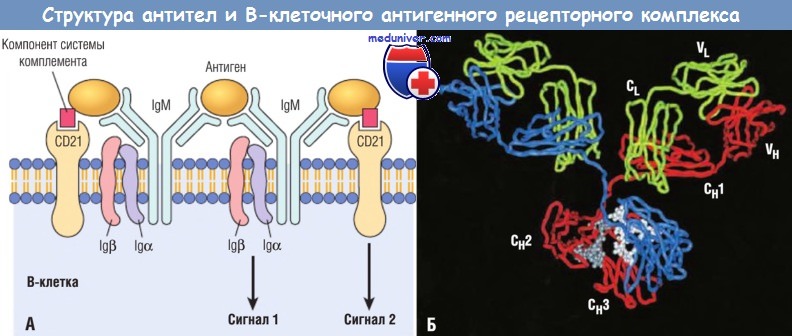
(А) В-клеточный рецепторный комплекс построен из мембранного иммуноглобулина М (IgM) (или IgD — не показан), распознающего антиген, и ассоциированных с ним сигнальных белков Iga и Igb.
CD21 представляет собой рецептор компонента системы комплемента, также способствующего активации В-клеток.
(Б) Кристаллическая структура секретируемой lgG-молекулы, показывающая расположение вариабельной (V) и константной (С) областей тяжелой (Н) и легкой (L) цепей.
г) Макрофаги. Макрофаги составляют часть системы мононуклеарных фагоцитов (их происхождение, дифференцировка и роль в воспалении обсуждены в отдельной статье на сайте (рекомендуем пользоваться формой поиска выше)). Здесь следует лишь подчеркнуть, что они выполняют важную функцию в индукции и эффекторной фазе приобретенного иммунного ответа, а именно:
- макрофаги, фагоцитировавшие микробы и белковые антигены, осуществляют процессинг антигенов и презентируют пептидные фрагменты Т-клеткам. Таким образом, в процессе активации Т-клеток макрофаги функционируют в качестве АПК;
- макрофаги являются ключевыми эффекторными клетками при некоторых формах клеточного иммунитета, элиминируя внутриклеточные микробы. При таком ответе Т-клетки активируют макрофаги и усиливают их способность уничтожать поглощенные микробы (см. далее);
- макрофаги участвуют также в эффекторной фазе гуморального иммунитета. Макрофаги активно фагоцитируют и разрушают микробы, опсонизированные IgG или С3b.
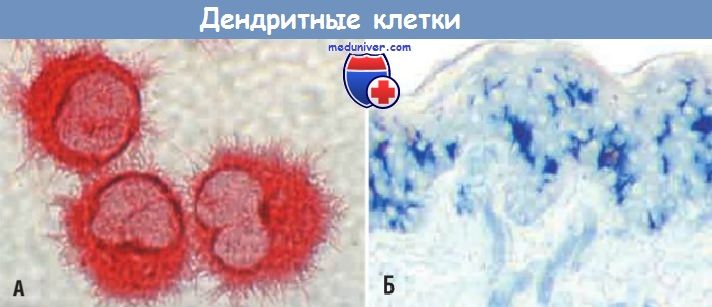
(А) Культивируемые дендритные клетки с хорошо видимыми поверхностными отростками.
(Б) Расположение клеток Лангерганса в эпидермисе (окрашены в синий цвет иммуногистохимическим методом.
д) Естественные клетки-киллеры. NK-клетки составляют 10-15% лимфоцитов периферической крови. Они не экспрессируют TCR или Ig. Морфологически NK-клетки несколько крупнее малых лимфоцитов и содержат большое число азурофильных гранул, поэтому их также называют большими гранулярными лимфоцитами. NK-клетки обладают способностью убивать инфицированные и опухолевые клетки, не нуждаясь в предварительном контакте с этими клетками или в активации под их влиянием. Эта способность делает NK-клетки первой линией защиты от вирусных инфекций и, возможно, от некоторых опухолей. Обычно для идентификации NK-клеток служат две молекулы на их поверхности — CD16 и CD56.
Молекула CD16 представляет собой Fc-рецептор для IgG, и благодаря ее присутствию NK-клетки приобретают способность лизировать опсонизированные IgG клетки-мишени. Этот феномен известен под названием антитело-зависимой клеточно-опосредованной цитотоксичности.
Функциональная активность NK-клеток регулируется балансом между сигналами, идущими от активирующих и ингибирующих рецепторов. Существует много типов активирующих рецепторов, из которых лучше всего изучено семейство NKG2D. Рецепторы NKG2D распознают поверхностные молекулы, индуцированные под влиянием различных видов стресса, таких как инфекция и повреждение ДНК. Ингибирующие рецепторы NK-клеток распознают собственные молекулы МНС класса I организма, экспрессируемые всеми нормальными клетками. Эти рецепторы принадлежат к двум главным семействам:
Ig-подобным рецепторам NK-клеток и семейству лектинов CD94 (белков, распознающих углеводы). Ингибирующие рецепторы предотвращают действие NK-клеток на неизмененные клетки. Вирусные инфекции или неопластическая трансформация часто индуцируют экспрессию клетками лигандов для активирующих рецепторов и в то же время снижают экспрессию молекул МНС класса I. В результате баланс сдвигается в сторону активации и инфицированные или опухолевые клетки уничтожаются.
NK-клетки секретируют также цитокины, в частности IFN-y, стимулирующий способность макрофагов разрушать микробы. Так макрофаги выполняют функцию ранней защиты от внутриклеточных микробных инфекций. Активность NK-клеток регулируют многие цитокины, включая IL-2, IL-12 и IL-15. IL-2 и IL-15 стимулируют пролиферацию NK-клеток, в то время как IL-12 активирует киллинг и секрецию IFN-y.
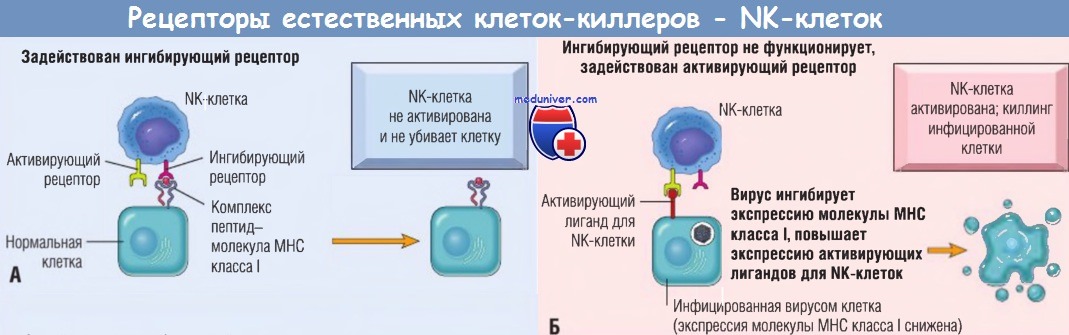
(А) Нормальные клетки экспрессируют молекулы класса I собственного главного комплекса гистосовместимости (МНС), распознаваемые ингибирующими рецепторами, благодаря чему NK-клетки не атакуют собственные клетки.
Обратите внимание, что здоровые клетки могут экспрессировать лиганды для активирующих рецепторов или не экспрессировать их (как показано), однако они не активируют NK-клетки,
т.к. взаимодействуют с ингибирующими рецепторами.
(Б) У инфицированных и подвергнутых стрессу клеток экспрессия молекул МНС класса I снижена, поэтому ингибирующие рецепторы не активируются и экспрессируются лиганды для активирующих рецепторов.
В результате NK-клетки активируются и убивают инфицированные клетки.
- Рекомендуем ознакомиться со следующей статьей "Органы иммунной системы"
Оглавление темы "Иммунная система":- Возможности ПЦР и методы оценки изменения последовательности ДНК
- Маркеры полиморфизма ДНК и их молекулярная диагностика
- Методы молекулярного анализа геномных изменений
- Эпигенетика и эпигенетические изменения
- Методы анализа РНК (рибонуклеиновой кислоты)
- Врожденный иммунитет и его характеристика
- Приобретенный иммунитет и его характеристика
- Клетки иммунной системы
- Органы иммунной системы
- Молекулы MHC - система презентации пептидов при приобретенном иммунном ответе

