Ишемическое и гипоксическое повреждение клеток
Выяснив причины, морфологию и механизмы развития повреждения клетки и некроза, рассмотрим теперь некоторые часто встречающиеся и очень важные для клиницистов формы повреждения клетки, заканчивающиеся некрозом. Эти примеры иллюстрируют множество механизмов и последовательность событий при повреждении клетки, описанном ранее.
Ишемическое и гипоксическое повреждение - наиболее распространенный тип повреждения клеток в клинической практике. Его изучали на животных, клеточных культурах и в исследованиях с участием людей. Гипоксия, развивающаяся в результате снижения доставки кислорода, может возникнуть при различных клинических состояниях. С другой стороны, при ишемии доставка кислорода и питательных веществ снижена чаще из-за снижения кровотока вследствие механической обструкции артериальной кровеносной системы, а также из-за уменьшения венозного оттока.
В отличие от гипоксии, во время которой может продолжаться выработка энергетических продуктов путем анаэробного гликолиза, при ишемии прекращается поставка субстратов для гликолиза. Таким образом, в ишемизированных тканях останавливается не только аэробный метаболизм, но и анаэробная выработка энергии после применения гликолитических субстратов или в результате блокирования гликолиза вследствие накопления метаболитов, которые должны удаляться с кровотоком.
По этой причине ишемия вызывает более быстрое и тяжелое повреждение клеток, чем гипоксия в отсутствие ишемии.
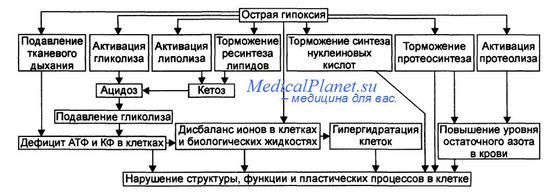
Механизмы ишемического повреждения клетки
Последовательность событий при гипоксии и ишемии отражает многие биохимические изменения, происходящие при повреждении клетки. Поскольку парциальное давление кислорода в клетках падает, нарушается окислительное фосфорилирование и снижается генерация АТФ. Истощение запасов АТФ приводит к отказу натриевого насоса, потере калия, входу в клетку натрия и воды и набуханию клетки.
В клетку входит много Са2+, что сопровождается множеством неблагоприятных эффектов, в частности увеличением потерь гликогена и снижением синтеза белков. Функциональные последствия на этой стадии могут быть тяжелыми. Например, сердечная мышца перестает сокращаться через 60 сек после коронарной окклюзии. Однако утрата сократительной способности не приравнивается к смерти клетки. Если гипоксия продолжается, усугубление истощения запасов АТФ вызовет дальнейшее повреждение.
Повреждение цитоскелета приводит к утрате таких ультраструктурных признаков, как микроворсинки, и формированию пузырьков на поверхности клетки. Миелиновые тельца, производные распавшихся клеточных мембран, могут быть обнаружены в цитоплазме (в аутофагических вакуолях) или вне клетки. Считается, что это результат немаскирующихся фосфатидных групп, запускающих захват и интеркаляцию воды между плоскими (ламинарными) мембранными массами. В это время митохондрии, как правило, набухают в результате утраты контроля объема в органеллах, ЭПР дилатируется, вся клетка набухает из-за увеличенного количества воды, натрия и хлора, а также снижается концентрация калия. Если на данном этапе поступление кислорода восстанавливается, все эти изменения оказываются обратимыми.
При продолжающейся ишемии повреждение становится необратимым и приводит к некрозу. Морфологически необратимое повреждение проявляется тяжелым набуханием митохондрий, обширным повреждением плазматической мембраны (с образованием миелиновых телец) и набуханием лизосом. В митохондриальном матриксе появляются большие, похожие на пучки шерсти аморфные включения — признак необратимого повреждения миокарда, который появляется через 30-40 мин от начала ишемии. Потом начинается массивный вход кальция в клетку, особенно при реперфузии.
Смерть клетки наступает в результате некроза, но апоптоз тоже участвует в этом процессе. Апоптоз активируется в большей степени вследствие высвобождения проапоптозных молекул из распадающихся митохондрий. Начинается прогрессирующая деградация компонентов клетки, и происходит выход ферментов в межклеточное пространство, а также вход макромолекул в погибающую клетку из интерстициального пространства. В итоге мертвые клетки замещаются массами, состоящими из фосфолипидов в форме миелиновых телец, которые подвергаются фагоцитозу и разрушаются до жирных кислот. Кальцификация таких остатков жирных кислот происходит с образованием кальциевых мыл.
Выход внутриклеточных ферментов и других белков через аномально проницаемую плазматическую мембрану в кровь — важный клинический признак смерти клеток. Например, повышенные уровни изофермента креатинкиназы-МВ и тропонина в крови являются первыми признаками инфаркта миокарда. Эти признаки можно обнаружить морфологически намного раньше, чем у больного будет диагностирован инфаркт.
Клетки млекопитающих могут формировать защитную реакцию на гипоксию. Подробнее всего описан гипоксия-индуцибелъный фактор 1, который индуцирует формирование новых кровеносных сосудов, стимулирует выживание клеток и запускает процесс анаэробного гликолиза.
Понимание кислород-чувствительных механизмов позволяет разработать новые стратегии для предотвращения и лечения ишемического или гипоксического повреждения клетки.
Несмотря на большое количество исследований и экспериментальных моделей, до сих пор нет однозначных терапевтических подходов, уменьшающих ишемические повреждения в клинических ситуациях. Наиболее используемая при ишемии (и травмах) головного мозга и повреждении спинного мозга стратегия — транзиторная индуцированная гипотермия (снижение температуры тела до 33,3°С). Этот метод снижает метаболические потребности клеток, уменьшает их набухание, предотвращает формирование свободных радикалов и блокирует воспалительную реакцию. Все это способствует уменьшению повреждения клетки и ткани.
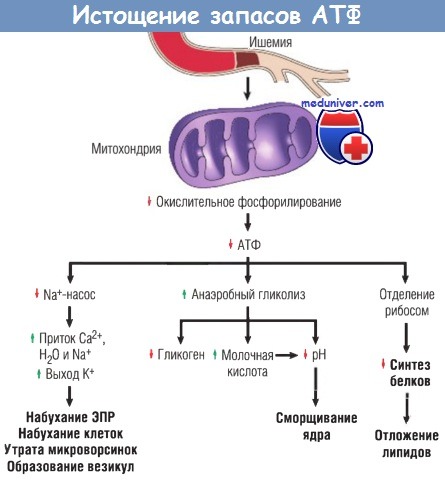
Морфологические изменения указывают на обратимое повреждение клетки.
Дальнейшее истощение запасов АТФ ведет к смерти клетки, обычно развивается некроз.
pH — водородный показатель; ЭПР — эндоплазматический ретикулум.
- Рекомендуем ознакомиться со следующей статьей "Реперфузионное повреждение клетки после ишемии"
Оглавление темы "Патология клетки":- Ишемическое и гипоксическое повреждение клеток
- Реперфузионное повреждение клетки после ишемии
- Механизмы химического повреждения клетки
- Что такое апоптоз? Причины апоптоза
- Морфологические изменения при апоптозе
- Биохимические признаки апоптоза
- Механизмы апоптоза и их патогенез
- Внутренний путь развития апоптоза
- Внешний путь развития апоптоза
- Механизмы запуска апоптоза
- Специфические свойства йоги Айенгара

