Механизмы развития (патогенез) иммуногемолитической анемии
Гемолитические анемии этого вида вызывают антитела, связывающиеся с эритроцитами, что приводит к преждевременному разрушению клеток. Это нарушение часто относят к аутоиммунным гемолитическим анемиям, но термин «иммуногемолитическая анемия» предпочтительнее, т.к. в некоторых случаях иммунную реакцию инициируют лекарственные средства.
Иммуногемолитические анемии можно классифицировать на основе характеристик ответственных за их возникновение антител.
Для постановки диагноза «иммуногемолитическая анемия» необходимо определение антител и/или компонентов системы комплемента на эритроцитах пациента. С этой целью применяют прямой антиглобулиновый тест Кумбса: эритроциты пациента смешивают с сыворотками, содержащими антитела, специфичные к Ig человека или компонентам системы комплемента.
Если на поверхности эритроцитов присутствует Ig или компонент системы комплемента, поливалентные антитела вызывают агглютинацию — видимые невооруженным глазом агрегаты клеток. При непрямом антиглобулиновом тесте Кумбса исследуют способность сыворотки пациента агглютинировать большое количество эритроцитов, покрытых определенными антигенами. Этот тест используют для характеристики антигена-мишени и определения температурной зависимости реагирующих с этим антигеном антител.
Существуют также иммунологические тесты для прямого количественного определения таких антител.

а) Анемии, индуцированные тепловыми антителами. Тепловые антитела (IgG, активные при температуре 37°С) служат наиболее частой причиной иммуногемолитических анемий. Около 50% таких анемий являются первичными (идиопатическими), другие обусловлены предрасполагающими факторами или действием лекарственных средств. В большинстве случаев каузальные антитела принадлежат к IgG, реже к IgA. Обычно наблюдается внесосудистый гемолиз. Эритроциты, покрытые IgG, связываются посредством Fc-рецепторов на фагоцитах, которые нарушают скелет мембраны эритроцитов частичным фагоцитозом, в результате, как и при наследственном сфероцитозе, эритроциты становятся сфероцитами, которые в селезенке быстро секвестрируются и удаляются.
Обычно обнаруживается умеренная спленомегалия из-за гиперплазии селезеночных фагоцитов.
Причина первичной иммуногемолитической анемии, как и других аутоиммунных заболеваний, неизвестна. В большинстве случаев антитела направлены против Rh-антигенов. Механизмы лекарственно-индуцированной иммуногемолитической анемии изучены лучше. Описаны два механизма:
- антигенные лекарственные средства. В этом случае гемолиз обычно начинается после внутривенного введения высоких доз лекарственного средства и манифестирует через 1-2 нед после начала терапии. Лекарственные средства, например пенициллин и цефалоспорины, связываются с мембраной эритроцитов и распознаются специфическими антителами. Иногда антитела связываются только с лекарственным средством, как при гемолизе, индуцированном пенициллином. В других случаях, в частности при гемолизе, вызванном хинидином, антитела распознают комплекс «лекарственное средство-мембранный белок».
Иногда антитела связывают компоненты системы комплемента, вызывая внутрисосудистый гемолиз, однако чаще действуют как опсонины, способствуя внесосудистому гемолизу внутри фагоцитов;
- лекарственные средства, нарушающие толерантность. Эти лекарственные средства, примером которых является антигипертензивный агент а-метилдопа, индуцируют неизвестным способом продукцию антител к антигенам эритроцитов, особенно к Rh-антигенам. Аутоантитела к а-метилдопе образуются у 10% пациентов, принимающих это лекарственное средство, и у 1% из них возникает клинически значимый гемолиз.
Лечение иммуногемолитической анемии, индуцированной тепловыми антителами, заключается в устранении инициирующих факторов (т.е. лекарственного средства). Если это невозможно, основой терапии становятся применение иммуносупрессивных препаратов и спленэктомия.
б) Анемии, индуцированные холодовыми агглютининами. Эту форму иммуногемолитических анемий индуцируют IgM, активные при температуре ниже 37°С (авидно связывающиеся с эритроцитами при температуре 0-4°С). Эти иммуногемолитические анемии встречаются реже, чем индуцированные тепловыми антителами, — в 15-30% случаев. Иногда холодовые агглютинины временно образуются после некоторых инфекций, вызываемых, например, М. pneumoniae, EBV, цитомегаловирусом, вирусом гриппа и ВИЧ.
В этих случаях расстройства являются самоограничивающимися и антитела редко вызывают клинически значимый гемолиз. Хроническая иммуногемолитическая анемия, индуцированная холодовыми агглютининами, встречается на фоне некоторых В-клеточных неоплазий или как идиопатическое расстройство.
Клинические симптомы обусловлены связыванием IgM с эритроцитами в сосудистом ложе, где температура может упасть ниже 30°С (например, при воздействии холода на пальцы рук, ног и уши). После связывания эритроциты агглютинируются и быстро связывают систему комплемента. По мере рециркуляции и нагревания крови IgM высвобождаются, обычно еще до того, как наступает опосредованный системой комплемента гемолиз. Однако преходящего взаимодействия с IgM достаточно для отложения сублитического количества С3b — превосходного опсонина, обеспечивающего удаление пораженных клеток фагоцитами в селезенке, печени и костном мозге.
Гемолиз может иметь различную степень тяжести. Сосудистая обструкция, вызванная агглютинированными эритроцитами, клинически проявляется бледностью, цианозом и феноменом Рейно в частях тела, подвергающихся воздействию низкой температуры.
Хроническую иммуногемолитическую анемию, индуцированную холодовыми агглютининами, лечить трудно.
Анемии, индуцированные холодовыми гемолизинами. Холодовые гемолизины вызывают пароксизмальную холодовую гемоглобинурию. Это редкое расстройство характеризуется значительным, иногда фатальным внутрисосудистым гемолизом и гемоглобинурией. Холодовые гемолизины принадлежат к классу IgG и связываются с Р-антигенами на поверхности эритроцитов в охлажденных периферических областях тела, т.е. активны при температуре ниже 37°С. Когда клетки, рециркулируя, попадают в более теплые центральные области организма, происходит опосредованный системой комплемента лизис, поскольку каскад активации системы комплемента эффективнее при 37°С. В большинстве случаев поражаются дети после вирусных инфекций. Обычно расстройство имеет преходящий характер и большинство заболевших детей выздоравливает в течение 1 мес.
в) Гемолитическая анемия вследствие травмы эритроцитов. Наиболее выраженный гемолиз вследствие травмы эритроцитов наблюдается у лиц с искусственными клапанами сердца и микроангиопатией. Механические клапаны сердца чаще служат причиной гемолиза по сравнению с биологическими протезами. Гемолиз происходит под влиянием сил сдвига, возникающих вследствие турбулентного тока крови, и градиента давления в поврежденных клапанах. Микроангиопатическая гемолитическая анемия чаще ассоциируется с диссеминированным внутрисосудистым свертыванием, однако встречается также при тромботической тромбоцитопенической пурпуре (ТТП), гемолитико-уремическом синдроме (ГУС), злокачественной гипертензии, СКВ и диссеминированной злокачественной опухоли.
Общим патогенным фактором при этих заболеваниях является поражение микрососудов, заключающееся в сужении их просвета, часто вследствие отложения фибрина и тромбоцитов. Сосудистые изменения вызывают напряжение сдвига, механически повреждающее проходящие клетки. Независимо от причины травматические повреждения приводят к появлению в мазках крови фрагментированных эритроцитов (шистоцитов), пойкилоцитов с шиповидными отростками, шлемовидных клеток и клеток треугольной формы.
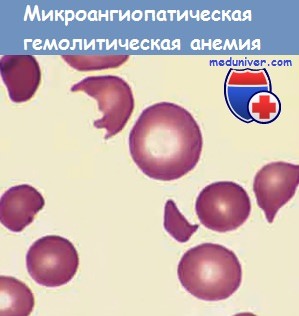
(мазок периферической крови пациента с гемолитико-уремическим синдромом).
Видно несколько фрагментированных эритроцитов.
- Рекомендуем ознакомиться со следующей статьей "Механизмы развития (патогенез) мегалобластной анемии"
Оглавление темы "Патогенез анемий":- Механизмы развития (патогенез) серповидно-клеточной анемии
- Механизмы развития (патогенез) бета-талассемии
- Механизмы развития (патогенез) альфа-талассемии
- Механизмы развития (патогенез) пароксизмальной ночной гемоглобинурии
- Механизмы развития (патогенез) иммуногемолитической анемии
- Механизмы развития (патогенез) мегалобластной анемии
- Механизмы развития (патогенез) пернициозной анемии
- Механизмы развития (патогенез) анемии при дефиците фолиевой кислоты
- Механизмы развития (патогенез) железодефицитной анемии
- Механизмы развития (патогенез) анемии из-за хронического заболевания

