Механизмы развития ВИЧ-инфекции - жизненный цикл ВИЧ
Хотя ВИЧ способен инфицировать многие ткани, существует две главные мишени для ВИЧ-инфекции: иммунная система и ЦНС.
Отличительный признак СПИДа — тяжелый иммунодефицит, в первую очередь затрагивающий клеточный иммунитет. Это обусловлено главным образом инфицированием и потерей Т-клеток CD4+, а также нарушением функции выживших хелперных Т-клеток. Как будет указано далее, макрофаги и дендритные клетки тоже являются мишенями для ВИЧ-инфекции. ВИЧ проникает в организм через слизистые оболочки и кровь, инфицируя в первую очередь Т-клетки, дендритные клетки и макрофаги.
Инфекция локализуется в лимфоидной ткани, где вирус может оставаться в латентном состоянии длительный период. Активная репликация вируса ассоциирована с увеличением числа инфицированных клеток и прогрессированием болезни с переходом в СПИД. Далее будут описаны механизмы проникновения вируса в Т-клетки и макрофаги и цикл репликации вируса в клетках, а затем — дан более детальный обзор процессов взаимодействия ВИЧ с его клеточными мишенями.
Жизненный цикл ВИЧ. Жизненный цикл вируса складывается из процесса инфицирования клеток, интеграции провируса в геном клеток организма-хозяина, активации вирусной репликации и образования и высвобождения вируса. Молекулы и механизмы каждого из этих этапов достаточно хорошо изучены.
1) Инфицирование клеток. ВИЧ инфицирует клетки, используя молекулу CD4 в качестве рецептора, а рецепторы различных хемокинов — как корецепторы. Необходимость связывания с CD4 объясняет избирательный тропизм вируса к Т-клеткам CD4+ и другим клеткам CD4+, особенно моноцитам/ макрофагам и дендритным клеткам. Однако связывания с CD4 еще недостаточно для инфицирования.
Белок gp120 вируса должен связаться и с другими молекулами клеточной поверхности (корецепторами), чтобы вирус смог проникнуть в клетки. Для этой цели служат рецепторы хемокинов, особенно CCR5 и CXCR4. Изоляты ВИЧ можно различить по использованию ими тех или иных рецепторов: штаммы R5 используют CCR5, штаммы Х4 — CXCR4, а некоторые штаммы (R5X4) обладают двойным тропизмом.
В 90% случаев ВИЧ типа R5 (М-тропный) представляет собой доминантный вирус, обнаруживаемый в крови недавно инфицированных индивидов и на ранней стадии инфекции. В процессе прогрессирования инфекции постепенно накапливаются Т-тропные вирусы, которые особенно вирулентны, т.к. способны инфицировать многие Т-клетки и даже тимусные предшественники Т-клеток, поражая и истощая пул Т-клеток.
С помощью исследований были выявлены молекулярные детали смертельно опасного взаимодействия гликопротеинов ВИЧ и их клеточных рецепторов. Эти взаимодействия могут лечь в основу разработки методов анти-ВИЧ-терапии. Оболочка ВИЧ содержит два гликопротеина — поверхностный белок gp120 и нековалентно связанный с ним трансмембранный белок gp41. Инициальный этап инфекции заключается в связывании гликопротеина оболочки gp120 с молекулами CD4. Это связывание вызывает конформационное изменение, приводящее к образованию нового участка распознавания на gp120 для корецепторов CCR5 или CXCR4.
Связывание с корецепторами индуцирует конформационные изменения gp41, в результате на конце gp41 экспонируется гидрофобная область, называемая пептидом слияния. Этот пептид встраивается в клеточную мембрану клеток-мишеней (т.е. Т-клеток или макрофагов), приводя к слиянию вируса с клетками организма-хозяина. После этого сердцевина вируса, содержащая геном ВИЧ, проникает в цитоплазму клетки. Необходимость связывания ВИЧ с корецепторами может иметь важное значение в патогенезе СПИДа. Хемокины препятствуют инфицированию ВИЧ клеточной культуры, связываясь со своими рецепторами.
Таким образом уровень хемокинов в тканях может влиять на эффективность вирусной инфекции in vivo. Полиморфизм гена, кодирующего CCR5, также ассоциирован с различной восприимчивостью к ВИЧ-инфекции. Около 1% американцев европеоидной расы наследуют две дефектные копии гена CCR5 и резистентны к инфекции и развитию СПИДа, ассоциированным с изолятами ВИЧ типа R5. Приблизительно 20% индивидов являются гетерозиготами по этому протективному аллелю CCR5; эти лица не защищены полностью от СПИДа, однако начало манифестации заболевания после инфицирования немного замедлено. В популяциях Африки и Восточной Азии гомозиготы по этой мутации встречаются редко.
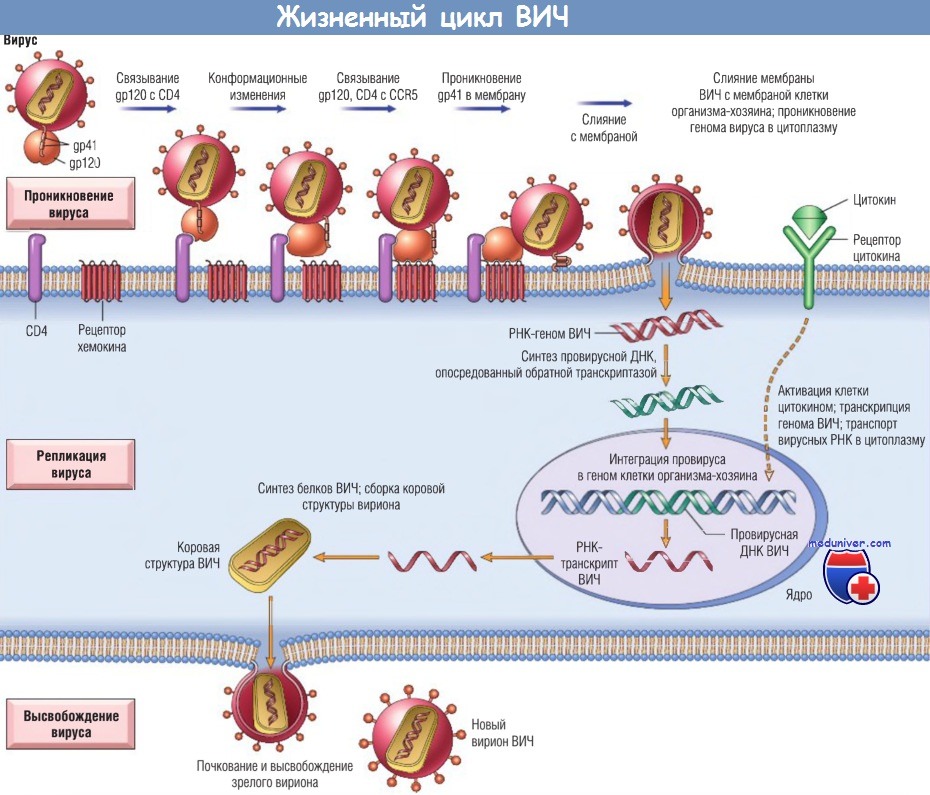
ВИЧ — вирус иммунодефицита человека; ДНК — дезоксирибонуклеиновая кислота; РНК — рибонуклеиновая кислота.
2) Репликация вируса. После интернализации геном вируса подвергается обратной транскрипции, приводя к синтезу двухцепочечной кДНК (провирусной ДНК). В покоящихся Т-клетках кДНК ВИЧ может оставаться в цитоплазме в линейной эписомной форме. В делящихся Т-клетках кДНК принимает кольцевидную форму, проникает в ядро и затем интегрируется в геном организма-хозяина.
После этой интеграции провирус может в течение нескольких месяцев или лет находиться в латентном состоянии. Возможна и другая ситуация, когда кДНК транскрибируется и образуются частицы полного вируса, отпочковывающиеся от клеточной мембраны. Такая продуктивная инфекция, ассоциированная с интенсивным почкованием вируса, приводит к смерти инфицированных клеток.
In vivo ВИЧ инфицирует Т-клетки памяти и активированные Т-клетки, однако не способен индуцировать продуктивное инфицирование наивных (неактивированных) Т-клеток. Наивные Т-клетки содержат активную форму фермента, вызывающего мутацию в геноме ВИЧ, — APOBEC3G. Это цитидиндезаминаза, индуцирующая мутации (цитозин => урацил) вирусной ДНК, образуемой в результате обратной транскрипции. Данные мутации ингибируют дальнейшую репликацию ДНК посредством еще не полностью понятных механизмов.
Активация Т-клеток превращает клеточный APOBEC3G в неактивный высокомолекулярный комплекс, что объясняет способность вируса к репликации в Т-клетках памяти (предварительно активированных) и Т-клеточных линиях. У ВИЧ выработался также механизм противодействия этому защитному клеточному механизму: вирусный белок Vif связывается с APOBEC3G и ускоряет его деградацию клеточными протеазами.
Завершение жизненного цикла вируса в латентно инфицированных клетках происходит лишь после клеточной активации. Активация большого числа инфицированных Т-клеток CD4+ приводит к их лизису. Активация Т-клеток антигеном или цитокинами повышает экспрессию нескольких факторов транскрипции, включая NF-кВ, которые стимулируют транскрипцию генов, кодирующих цитокины, например IL-2 и его рецептор. В покоящихся Т-клетках NF-kB секвестрирован в цитоплазме в комплексе с белком ингибитором каппа В (1кВ). Клеточная активация антигеном или цитокинами индуцирует цитоплазматические киназы, фосфорилирующие 1кВ.
В результате комплекс становится мишенью для ферментативного расщепления, а NF-кВ высвобождается и перемещается в ядро. В ядре он связывается с последовательностями промоторной области различных генов, включая гены цитокинов, которые экспрессируются в активированных Т-клетках. Длинные концевые повторы последовательности, фланкирующие геном ВИЧ, содержат и NF-кВ-связывающие участки, которые могут быть активированы теми же факторами транскрипции.
Теперь представим себе латентно инфицированную клетку CD4+, на которую действует антиген окружающей среды. Индукция NF-кВ в такой клетке (физиологический ответ) активирует транскрипцию провирусной ДНК ВИЧ (патологическое следствие) и в конечном итоге приводит к продукции вирионов и лизису клетки. Далее TNF и другие цитокины, образуемые активированными макрофагами, также стимулируют активность NF-кВ и тем самым приводят к продукции РНК ВИЧ.
Таким образом, оказывается, что ВИЧ-инфекция «цветет», когда Т-клетки и макрофаги организма-хозяина физиологически активированы. Такая активация in vivo может произойти в результате антигенной стимуляции самим ВИЧ или другими инфицирующими микроорганизмами. Инфицированные ВИЧ индивиды имеют повышенный риск развития других инфекций, приводящих к повышенной активации лимфоцитов и продукции провоспалительных цитокинов. В свою очередь, эти цитокины стимулируют дальнейшую продукцию ВИЧ, смерть образующихся Т-клеток CD4+ и усиление инфекции. Так у больных СПИДом возникает порочный круг и в итоге происходит неизбежное разрушение иммунной системы.
- Рекомендуем ознакомиться со следующей статьей "Механизмы иммунодефицита при ВИЧ-инфекции"
Оглавление темы "Заболевания иммунной системы":- Механизмы развития синдрома гипер-IgM
- Механизмы развития синдрома Ди Джорджи (гипоплазии тимуса)
- Механизмы развития тяжелого комбинированного иммунодефицита (ТКИД)
- Механизмы развития иммунодефицита с тромбоцитопенией и экземой (синдрома Вискотта-Олдрича)
- Механизмы развития генетической недостаточности системы комлемента
- Вторичные иммунодефициты и их характеристика
- Распространенность СПИД (ВИЧ) и группы риска
- Свойства ВИЧ и его строение
- Механизмы развития ВИЧ-инфекции - жизненный цикл ВИЧ
- Механизмы иммунодефицита при ВИЧ-инфекции

