Механизмы безграничного потенциала деления клеток
Каждая нормальная клетка человека может совершить 60-70 делений. После этого она теряет способность делиться и стареет. Данный феномен ассоциируется с прогрессирующим укорочением теломер, располагающихся на концах хромосом.
Предполагается, что короткие теломеры распознаются аппаратом восстановления ДНК как разрывы двухцепочечной ДНК, что приводит к остановке клеточного цикла посредством активации р53 и RB. В клетках, в которых точки контроля не функционируют из-за мутаций р53 или RB1, активируется негомологичный сигнальный путь присоединения «конец в конец» коротких концов двух хромосом как последнее отчаянное усилие по спасению клетки.
Такое восстановление ДНК приводит к децентрализации хромосом, которые растягиваются частично в анафазе, и появляются новые разрывы двухцепочечной ДНК. Возникающая в результате повторных разрывов мостиков ДНК нестабильность генома в конечном счете приводит к митотической катастрофе в виде массовой смерти клеток. Из этого следует, что для бесконечного роста опухоли недостаточно потерять только факторы ограничения роста.
Клетки опухоли также должны избежать старения и митотической катастрофы. Если клетке удается реактивировать теломеразу, повторные поломки мостиков ДНК прекращаются и клетка в состоянии избежать смерти. Однако во время периода геномной нестабильности, который предшествует активации теломеразы, могут накапливаться многочисленные мутации, приводящие к злокачественной трансформации клетки. Прохождение через период геномной нестабильности, вероятно, объясняет появление сложных кариотипов, часто обнаруживаемых в карциномах у человека.
Теломераза активна в нормальных стволовых клетках, но в большинстве зрелых соматических клеток обычно отсутствует или присутствует в очень небольшом количестве. В отличие от этого модификация теломер обнаруживается фактически во всех типах опухолей. В 85-95% новообразований это происходит из-за повышенной активности фермента теломеразы.
Некоторые опухоли используют другие механизмы, названные альтернативным удлинением теломер, которые, вероятно, зависят от рекомбинации ДНК. Интересно, что в процессе прогрессирования аденомы толстой кишки до аденокарциномы толстой кишки ранние этапы характеризуются высокой степенью геномной нестабильности с низкой экспрессией теломеразы, тогда как злокачественные новообразования на более поздних сроках развития имели сложные кариотипы с высокими уровнями активности теломеразы, что сопоставимо с моделью теломер-управляемого онкогенеза злокачественных опухолей человека.
Некоторые другие механизмы геномной нестабильности будут обсуждены далее.
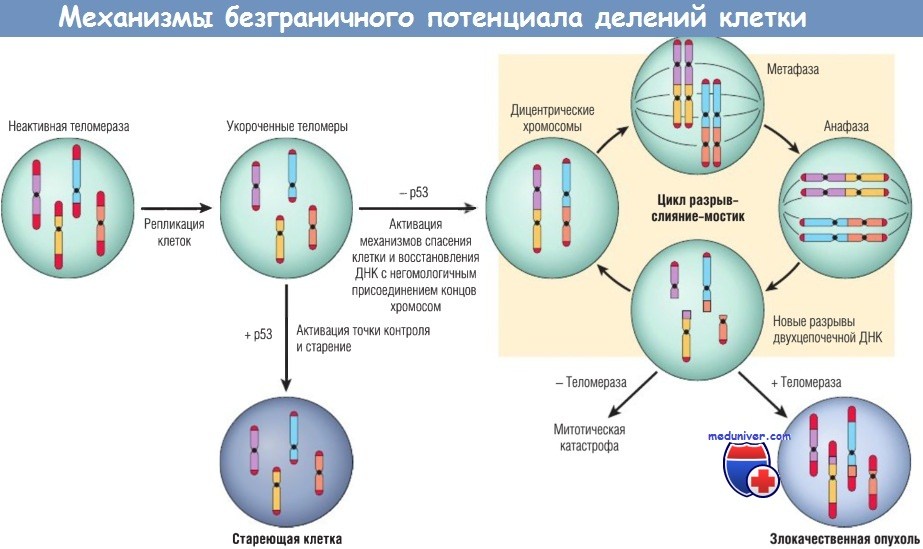
Репликация соматических клеток, которые не экспрессируют теломеразы, приводит к укорочению теломер. При функционирующих точках контроля клетки с укороченными теломерами входят в фазу старения.
В отсутствие функционирующих точек контроля активируется неадекватный путь восстановления ДНК, приводя к формированию дицентрических хромосом.
Во время митоза эти хромосомы растягиваются, в результате происходят разрывы двухцепочечной ДНК, которые активируют восстановление ДНК, приводя к случайным соединениям концов хромосом.
Клетки подвергаются многочисленным повторениям этого цикла, что приводит к массивной хромосомной нестабильности и многочисленным мутациям.
Если клетка не в состоянии повторно экспрессировать теломеразу, то наступает митотическая катастрофа и смерть.
Реэкспрессия теломеразы позволяет клеткам избежать цикла поломки и восстановления ДНК с присоединением концов хромосом, таким образом сохраняется жизнеспособность и стимулируется онкогенез.
- Рекомендуем ознакомиться со следующей статьей "Механизмы ангиогенеза опухоли"
Оглавление темы "Патофизиология опухоли":- Ген PTEN и его значение в развитии опухоли
- Гены NF1, NF2 и их значение в развитии опухоли
- Ген VHL и его значение в развитии опухоли
- Ген WT1 и его значение в развитии опухоли
- Ген PTCH и его значение в развитии опухоли
- Механизмы уклонения клеток опухоли от апоптоза
- Механизмы безграничного потенциала деления клеток
- Механизмы ангиогенеза опухоли
- Механизмы инвазии опухоли
- Механизмы гематогенного метастазирования опухоли по сосудам

