Тенасцин внеклеточного матрикса. Взаимодействие матриксных молекул
Тенасцин — олигомерный гликопротеид с молекулярной массой более 100 000, обладает адгезивными и антиадгезивными свойствами [Faissnen U., Kruse М., 1990]. Его молекула имеет мозаичную структуру, включающую ЭФР-подобные повторы, RGD-последовательности и Са2+-связывающие домены [Erickson D., Kruse М., 1990].
Молекула тромбосподина содержит глобулярные С- и N-kohцевые домены, которые вовлекаются в связывание Са2+ и гепарина. Эти области также взаимодействуют с коллагеном, фибронектином, фибриногеном, ламинином и плазминогеном [Asch R., Nachman J., 1989]. Тромбосподин может взаимодействовать с гепарансульфатом, интегринами, гликопротеидом IV, сульфатированными гликолипидами, но это взаимодействие происходит не во всех клетках [Prater R. et al., 1989]. Тромбосподин описан как адгезивный белок для кератиноцитов, клеток меланомы и тромбоцитов. В эндотелии и фибробластах он проявляет свои антиадгезивные свойства. Возможным объяснением такого спектра действия является способность тромбосподина связывать ТФРр [MurphyUllrich Ch. et al., 1990].
Тенасцин и тромбосподин формируют комплексы с протеогликанами, которые могут изменять их адгезивные свойства, В частности, ингибирующее влияние тенасцина проявляется только при его аффинной связи с хондроитинсульфатом.
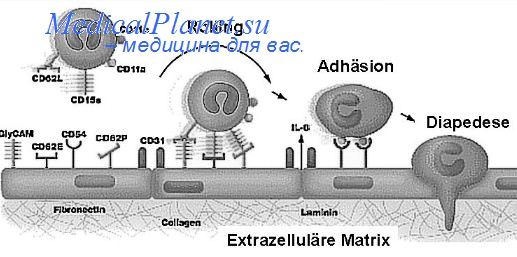
Таким образом, группа поверхностных и внеклеточных компонентов ЭЦМ может быть расширена за счет включения в нее SPARC и тромбосподина, которые связывают ТФРр и тромбоци-тарный фактор роста (ТцФР), а также эффективно тормозят их взаимодействие с клеточными рецепторами [Lane J. W. et al., 1991]. Клетки в контакте с макромолекулами ЭЦМ в условиях in vitro реагируют по-разному: иногда высокоселективно и быстро, иногда медленно и неспецифично. Эффект взаимодействия компонентов ЭЦМ с клетками во многом зависит от типа клеток и структуры ЭЦМ.
Молекулы фибронектина, перекрестно связываясь друг с другом через дисульфидные мостики, образуют фибриллярные структуры. Протеогликаны самоагрегируют при взаимодействии гликозаминогликановых цепей. Известна способность фибриллярных коллагенов спонтанно формировать ячеистые структуры. Для образования фибриллярной структуры требуются дополнительные химические изменения, включающие гликозилирование, протеолиз белков и гидроксилизирование некоторых остатков [Fessler M., Fessler R., 1978]. Коллаген IV типа спонтанно формирует уникальную сетеподобную структуру, хорошо выявляемую в БМ.
Так, одна из наиболее важных молекул взаимодействия в супрамолекулярной структуре, фибронектин, связывается только с денатурированным коллагеном I типа (желатином) [Engvald J. R., Ruoslahti E., 1977]. Фибронектин хуже связывается с тройной спиралевидной структурой коллагена, подтверждая тот факт, что места связывания вблизи С-конца маскированы в нативной молекуле. Другие коллагены и Clq-компонент также связывают фибронектин.
- Читать далее "Взаимосвязи фибронектина, ламинина и протеогликанов. Хондроитин и дерматансульфат"
Оглавление темы "Антигены и молекулы клеточного взаимодействия":1. Антиген CD26, CD73. Антиген лейкоцитов CD2
2. Молекула CD28. Концепция о ко-стимуляции
3. Коллаген IV типа. Ламинин
4. Нидоген энтактин. Фибронектин
5. Протеогликаны клеточных мембран. Молекулы внеклеточного матрикса
6. Тенасцин внеклеточного матрикса. Взаимодействие матриксных молекул
7. Взаимосвязи фибронектина, ламинина и протеогликанов. Хондроитин и дерматансульфат
8. Фибробласты. Распространенные медиаторы - цитокины
9. Взаимодействие клеток с иммунной системой. Интерлейкин-1
10. Синтез цитокинов. Фактор некроза опухоли (ФНО)

