Механизмы декомпенсации при гипертрофии сердца.
Потенциальные возможности гипертрофированного миокарда увеличивать силу и скорость сокращения не беспредельны. Если на сердце продолжает действовать повышенная нагрузка или оно дополнительно повреждается, сила и скорость его сокращений падают, а их энергетическая «стоимость» возрастает: развивается декомпенсация гипертрофированного сердца.
Механизмы декомпенсации гипертрофированного сердца перечислены на рисунке.
В основе декомпенсации длительно гипертрофированного миокарда лежит нарушение сбалансированности роста различных его структур. Эти сдвиги — наряду с другими — в конечном счёте обусловливают уменьшение силы сердечных сокращений и скорости контрактильного процесса, т.е. развитие сердечной недостаточности.
Клеточно-молекулярные механизмы сердечной недостаточности
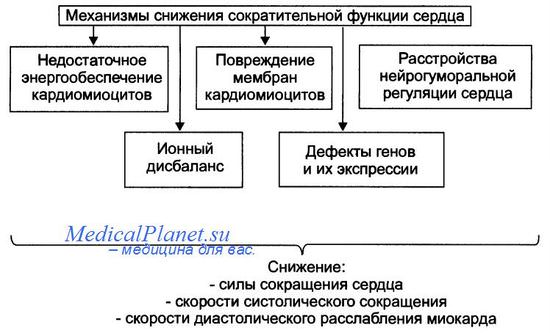
Снижение сократительной функции сердца является итогом развития сердечной недостаточности самой разной этиологии. Несмотря на различие причин и известное своеобразие начальных звеньев патогенеза сердечной недостаточности, её механизмы на клеточном и молекулярном уровне едины. Главные из этих механизмов приведены на рисунке.
• Недостаточность энергетического обеспечения клеток миокарда
Расстройство энергоснабжения основных процессов, происходящих в клетках миокарда (прежде всего его сокращения и расслабления), развивается вследствие нарушения ресинтеза макроэргов, транспорта их энергии к эффекторным структурам кардиомиоцитов, утилизации ими энергии макроэргических фосфатных соединений. Эти звенья патогенеза в общем виде рассмотрены в статье «Патология клетки».
Нарушение обеспечения кардиомиоцитов энергией на этапах её продукции, транспорта и утилизации может быть как стартовым механизмом снижения сократительной функции сердца, так и существенным фактором нарастания её депрессии.

• Повреждение мембран и ферментов кардиомиоцитов
Повреждение клеточных мембран и ферментов рассмотрено в статье «Патология клетки».
Альтерация мембран и ферментов клеток миокарда — главное, а нередко и инициальное звено патогенеза сердечной недостаточности. Изменение физико-химических свойств и конформации молекул белка (структурных и ферментов), липидов, фосфолипидов и ЛП сопровождается значительным обратимым, а часто — необратимым повреждением структуры и функции мембран и ферментов, в том числе митохондрий, саркоплазматического ретикулума, миофибрилл, плазматической мембраны, обеспечивающих реализацию сократительной и ритмической функций сердца.
• Ионный дисбаланс
Нарушение содержания и соотношения между отдельными ионами внутри и вне клеток рассмотрены в статье «Патология клетки». Ниже приведены специфичные для развития сердечной недостаточности особенности ионного дисбаланса.
Ионный дисбаланс при сердечной недостаточности проявляется нарушением соотношения между отдельными ионами в разных секторах кардиомиоцитов: в органеллах (митохондриях, саркоплазматическом ретикулуме, миофибриллах), в цитозоле, по разные стороны плазматической мембраны кардиомиоцитов. В наибольшей степени это относится к ионам: К+, Na+, Ca2+. Именно эти катионы в основном определяют реализацию таких процессов, как возбуждение, электромеханическое сопряжение, сокращение и расслабление миокарда.
• Нарушения в генетической программе кардиомиоцитов
Нарушения в генетической программе клеток и/или механизмов её реализации рассмотрены в статье «Патология клетки».
При сердечной недостаточности происходит активация генов, контролирующих процессы обновления субклеточных структур кардиомиоцитов, а также роста сосудов микроциркуляторного русла и нервных волокон. В частности, при ишемическом и стрессорном повреждении сердца подавлена экспрессия мРНК для Са2+-зависимой АТФазы саркоплазматической сети. Это и потенцирует ингибирование процессов захвата и выброса Са2+ ретикулумом миоцитов. В условиях ишемии и инфаркта миокарда, хронического эмоционально-болевого стресса подавлен также процесс трансляции генетической информации. Это сопровождается нарушением синтеза различных белков клеток миокарда.
• Расстройства нейрогуморалыюй регуляции сердца
Общая характеристика нарушений регуляции клеточных функций приведена в статье «Патология клетки». Ниже рассмотрены важные для развития сердечной недостаточности изменения симпатической и парасимпатической регуляции сердца.
+ Изменение механизмов симпатической регуляции.
- Уменьшение содержания нейромедиатора симпатической нервной системы — норадреналина в ткани сердца.
Причины. Снижение синтеза норадреналина в нейронах симпатической нервной системы (в норме в них образуется около 80% медиатора, содержащегося в миокарде). Является результатом подавления активности фермента тирозингидроксилазы и торможения захвата норадреналина нервными окончаниями.
- Снижение адренореактивных свойств сердца, т.е. выраженности ино-, хроно-, дромо- и батмотропных эффектов норадреналина и адреналина.
+ Изменение механизмов парасимпатической регуляции.
- Ацетилхолин через м-холинорецепторы вызывает уменьшение частоты сердечных сокращений, ингибируя образование цАМФ и активируя образование цГМФ который, в свою очередь, активирует цГМФ-зависимую киназу, подавляющую активность потенциалозависимых Са2+-каналов.
- Изменение механизмов парасимпатической регуляции при сердечной недостаточности выражено значительно меньше, чем симпатической. Это является результатом более высокой резистентности парасимпатических механизмов к различным повреждающим факторам.
Последствия нарушенных симпатических и парасимпатических влияний на миокард состоят в снижении степени управляемости и надёжности регуляции сердца. Это приводит к падению темпа и величины мобилизации сократительной функции сердца, особенно в чрезвычайных условиях.
Видео этиология, патогенез сердечной недостаточности систолической, диастолической, лево- и правожелудочковой
- Читать далее "Проявления сердечной недостаточности."
Оглавление темы "Сердечная недостаточность.":- Сердечная недостаточность. Причины сердечной недостаточности.
- Виды сердечной недостаточности.
- Механизмы развития сердечной недостаточности.
- Механизмы декомпенсации при гипертрофии сердца.
- Проявления сердечной недостаточности.
- Острая сердечная недостаточность. Отек легких.
- Хроническая сердечная недостаточность.
- Диастолическая сердечная недостаточность. Принципы нормализации функции сердца при его недостаточности.

